新冠病毒基因序列于2020年1月11日发布后,在全球科研界掀起了一波波疫苗研发浪潮。流行病防范创新联盟(CEPI)正与全球卫生当局和疫苗开发商合作,以支持新冠疫苗的开发。
日前,《自然》甚至对疫苗开发活动进行了全景式的概述。其提供的全景数据库包括通过WHO权威且不断更新的清单报告的疫苗开发计划,以及从公开可获得的专有资源中识别出的其他项目。概况提供了对COVID-19疫苗研发关键特征的见解,并为CEPI进行持续资产组合管理提供了参考资源。

《自然》还与全球健康生态系统中的其他人共享了这些信息,以帮助改善新冠肺炎疫情应对中的协调性,并使全球资源和能力针对最有希望的候选疫苗。
COVID-19疫苗研发概况
截至2020年4月8日,全球新冠疫苗的研发全景图谱中包含115种候选疫苗(图1),其中78种已确认处于推进状态,37种尚未确认(无法从公开可获得的信息或专有信息来源确定其开发状态)。在已确认的78个在研项目中,目前有73个处于探索或临床前阶段。最近最先进的候选药物已进入临床研究,包括来自Moderna的mRNA-1273,来自康希诺(CanSino Biologicals)的Ad5-nCoV,来自Inovio的INO-4800,LV-SMENP-DC和来自深圳市免疫基因治疗治疗研究院的LV-SMENP-DC 和病原体特异性aAPC(表1)。其他许多疫苗开发商也表示,计划在2020年内启动人体测试。
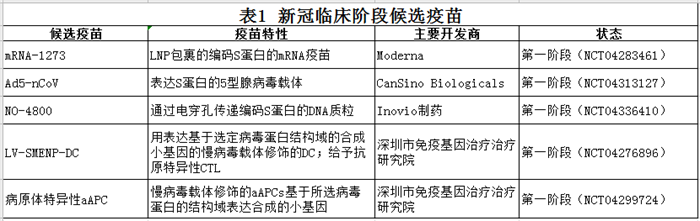
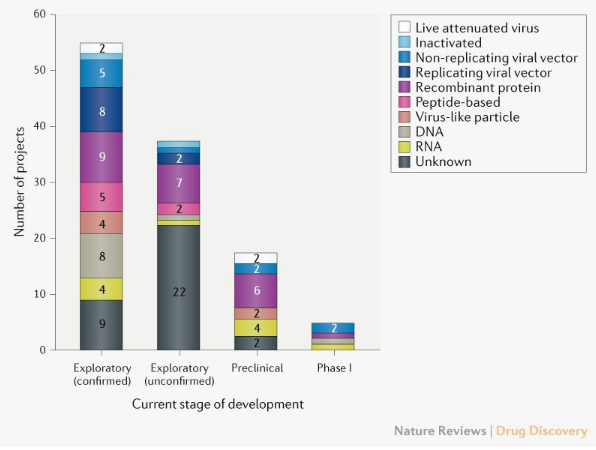
图1 通过技术平台的候选新冠疫苗渠道。探索性项目(分为已确认和未确认)处于早期计划阶段,没有进行体内测试,而临床前项目则处于体内测试和/或制造临床试验材料的阶段。(APC,人工抗原呈递细胞; CTL,细胞毒性T淋巴细胞; DC,树突状细胞; LNP,脂质纳米颗粒; S蛋白,SARS-CoV-2刺突蛋白。)资料来源:ClinicalTrials.gov网站; WHO。
技术平台的多样性
新冠疫苗开发前景的一个显著特征,是所涉及的技术平台范围广泛,包括核酸(DNA和RNA)、病毒样颗粒、肽、病毒载体(可复制和不可复制)、重组蛋白、减毒活疫苗和灭活疫苗等方法(图1)。这些平台中,许多目前都不是获得许可的疫苗的基础,但是在肿瘤学等领域的经验正在鼓励开发人员利用下一代方法提供的机会,以提高开发和制造的速度。可以想象,某些疫苗平台可能更适合特定人群的亚型(例如老年人、儿童、孕妇或免疫功能低下的患者)。
考虑到表1中的候选对象,基于DNA或mRNA的新型平台在抗原操作和速度潜力方面提供了极大的灵活性。实际上,在序列鉴定仅两个月后,Moderna就开始对其基于mRNA的疫苗mRNA-1273进行临床测试。基于病毒载体的疫苗可提供高水平的蛋白质表达和长期稳定性,并诱导强烈的免疫反应。最后,已经有针对其他疾病的基于重组蛋白的许可疫苗,因此此类候选药物可以利用现有的大规模生产能力。
对于某些平台,佐剂可以增强免疫原性并使较低的剂量可行,从而可以在不损害保护的情况下为更多人接种疫苗。到目前为止,至少有10个开发人员已表示计划开发针对COVID-19的佐剂疫苗,包括葛兰素史克、Seqirus和Dynavax在内的疫苗开发商已承诺将许可的佐剂(分别为AS03、MF59和CpG 1018)用于新冠疫苗。
有关疫苗开发中使用的特定新冠病毒抗原的公共信息有限。可获得信息的大多数候选药物旨在诱导针对病毒刺突(S)蛋白的中和抗体,从而防止通过人ACE2受体摄取。然而,尚不清楚用于不同候选物中的S蛋白的不同形式和/或变体如何相互关联,或与疾病的基因组流行病学之间如何关联。SARS疫苗开发的经验表明,不同抗原具有增强免疫力的潜力,这是一个有争议的话题,可能与疫苗开发有关。
疫苗开发商全景图
在确认的活性候选疫苗候选项目中,有56个(72%)由私人/工业开发商开发,其余22个项目(28%)由学术、公共部门和其他非营利组织牵头(图2)。
尽管许多大型跨国疫苗开发人员(如杨森、赛诺菲、辉瑞和葛兰素史克)都从事新冠疫苗的开发,但许多主要开发人员规模较小和/或缺乏大规模疫苗生产的经验。因此,重要的是确保疫苗生产与供应能力以及满足需求的能力之间的协调。
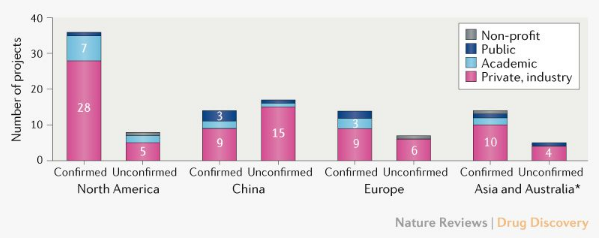
图2 按类型和地理位置划分的新冠疫苗开发商的资料。对于合伙企业,地点是主要开发商的所在地。 *中国除外。
大多数新冠苗开发活动都在北美,已确认活性疫苗候选者的开发者为36家(46%),而中国为14家(18%),亚洲(不包括中国)和澳大利亚为14家(18%),以及欧洲有14家(18%)(图2)。据报道,中国在疫苗开发方面还有更多努力,CEPI正在与中国科学技术部对话以确认其地位。
活跃的新冠候选疫苗的主要开发者分布在19个国家/地区,这些国家合计占全球人口的四分之三以上。但是,尽管在这些地区存在疫苗生产能力和监管框架,但目前在非洲或拉丁美洲尚无关于疫苗开发活动的公共信息。
新冠的流行病学可能因地理位置而异,有效控制这种流行病可能需要南半球加强协调并参与疫苗研发工作。
前景与展望
就规模和速度而言,针对新冠肺炎大流行的全球疫苗研发工作是前所未有的。
考虑到速度的紧迫性,有迹象表明,到2021年初,可以在紧急情况下使用疫苗或采取类似的协议,这将是传统疫苗开发路径的根本性转变——传统的疫苗开发路径平均需要10年以上的时间。不过,这还需要涉及并行和适应性开发阶段、创新的监管流程和扩大生产能力的新型疫苗开发范例。
传统疫苗开发范例的行业基准引用了许可疫苗的损耗率超过90%。针对性的新冠开发方法(其中涉及新的病毒靶标,通常还包括新颖的疫苗技术平台和新颖的开发范例)可能会增加与提供许可疫苗有关的风险,并且需要仔细评估有效性和每个步骤的安全性。
为了评估疫苗功效,正在开发新冠特定动物模型,包括ACE2转基因小鼠、仓鼠、雪貂和非人类灵长类动物。涉及活病毒挑战的动物研究需要生物安全级别3的封锁措施,对这些功能的需求可能需要国际协调,以确保有足够的实验室规模和能力。
最后,需要疫苗开发商、监管机构、政策制定者、资助者、公共卫生机构和政府之间进行强有力的国际协调与合作,以确保可以生产出足够数量的有前途的晚期候选疫苗,并公平地供应给所有受影响地区,特别是低产量地区资源区域。
CEPI最近发出了一项募集资金的呼吁,以支持全球新冠疫苗开发工作,该工作要遵循三个必要条件:速度、大规模生产和部署,以及全球可用性。CEPI表示,将保持动态的项目组合管理方法,并将在全球范围内提供支持的科学资源。同时,呼吁全球疫苗界集体动员必要的技术和财政支持,以通过全球疫苗接种计划成功应对新冠大流行,并为应对未来的流行病提供坚实的基础。
参考来源:https://www.nature.com/articles/d41573-020-00073-5
